【临研之声】临床研究注册与备案同步!国家医学研究登记备案信息系统解锁新功能
来源:临床医学研究中心 发布时间:2023年12月8日
相信近期关注临床研究备案要求的同行们都看到了这个利好的消息!
新功能一:减负进行时!
11月12日起,国家医学研究登记备案信息系统(www.medicalresearch.org.cn)与中国临床试验注册中心网站(www.chictr.org.cn)对接试运行,公告如下:
敲黑板|划重点
1、如何实现临床研究注册和备案同步?
11月12日试运行以后首次在国家医学研究登记信息备案系统登记者,只要在“是否需在‘中国临床试验注册中心网站’公开”选择“是”,并完成提交、机构审核等步骤即可。
11月12日试运行以前登记者,如果曾经选择了需在“中国临床试验注册中心网站”公开,应作项目变更,需补充填写注册相关的数据后再次提交、完成机构审核等步骤即可。
2、在国家医学研究登记信息备案系统登记前,已经在公认网址注册,并获得注册号的是否还要再填一次信息?
已经在中国临床试验注册中心、clinicaltrials等注册网址注册的研究者,请:
(1)在“是否需在‘中国临床试验注册中心网站’公开”――选择“否”
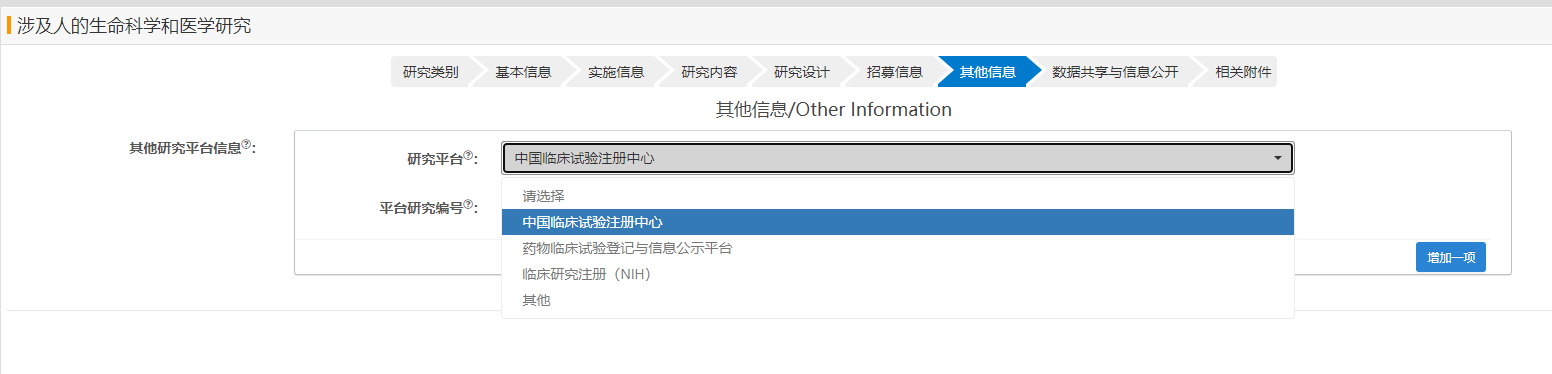
(2)在“其他研究平台信息”中选择对应的注册平台,并登记“平台注册编号”。
3、什么是注册?为什么要注册?是否一定要选择在‘中国临床试验注册中心网站’公开信息?
注册是期刊发表的要求。
国际医学期刊编辑委员会(ICMJE)在2004年提出,所有前瞻性、涉及人的干预性临床研究在期刊发表的前提是在第一例受试者纳入前在公认注册机构完成注册(应获得注册号)。截至2025-2026 年,全球超过5570种期刊遵守ICMJE要求,包括中华医学会下等中文期刊。因此,对于研究者而言,若在入组第一例受试者前未完成注册,将可能面临被期刊拒稿的风险!
ICMJE对于需要注册研究定义为:任何前瞻性,涉及人的干预性研究。不管是否设置试验组或对照组,干预措施是指用于改变生物医学或健康相关结果的措施,包括药物、手术、器械、行为治疗、教育计划、饮食干预、质量改进干预和护理过程的改变。健康结果是在患者或参与者中获得的任何生物医学或健康相关指标,包括药代动力学指标和不良事件。
ICMJE认可的临床研究注册平台一共有18个,注册只需要在其中任一平台完成即可。国内常用的注册平台包括中国临床试验注册中心(https://www.chictr.org.cn)和美国临床试验注册库(https://clinicaltrials.gov)。
新功能二:免费大礼包!
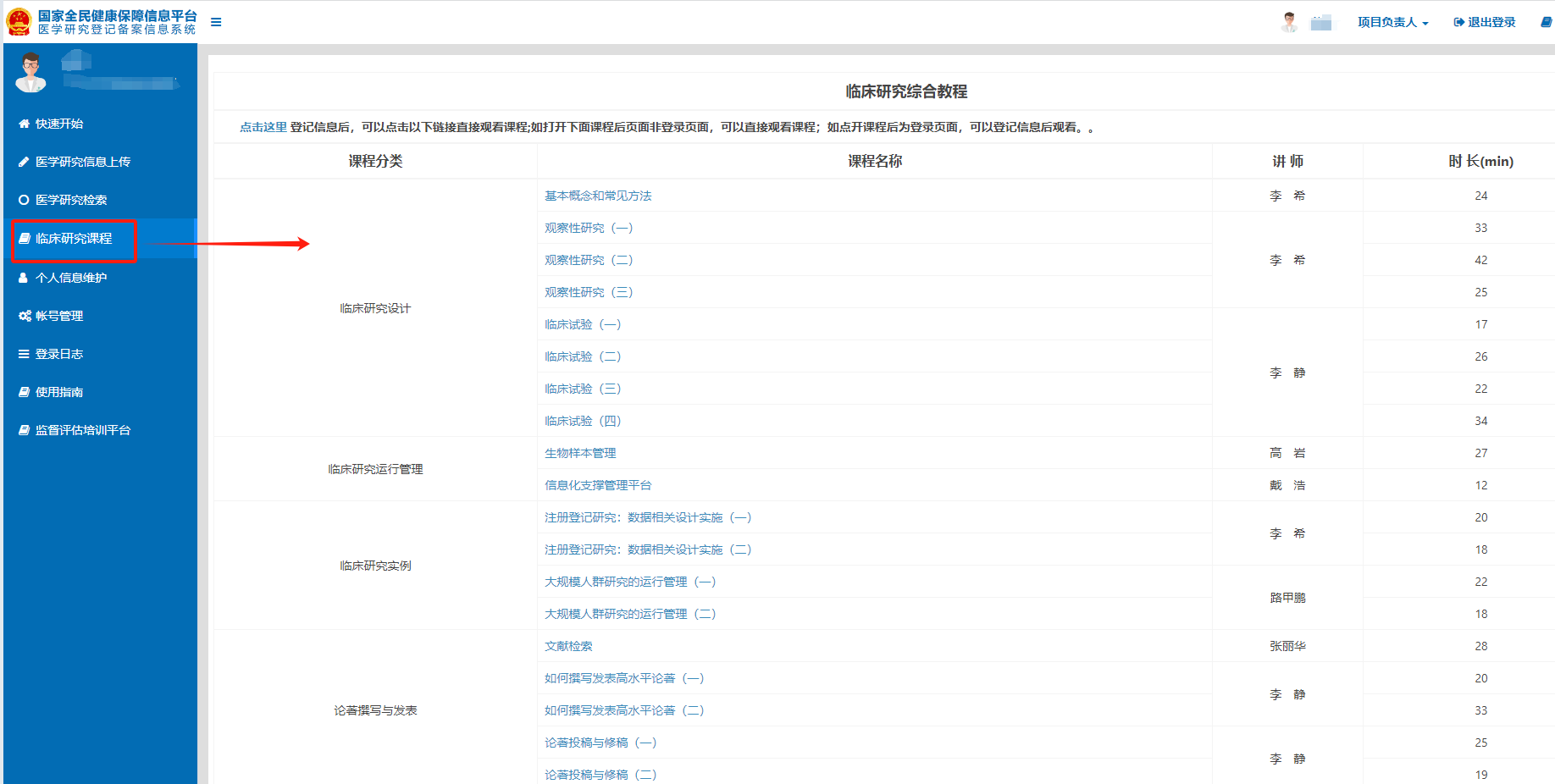
10月26日起,国家医学研究登记备案信息系统上线临床研究培训课程,内容覆盖:临床研究设计、临床研究运行管理、临床研究实例、论著撰写发表共4类19节课。
撰文:张怡(中山大学孙逸仙纪念医院)
审核:曹烨(中山大学肿瘤防治中心)
编辑:广东省临床医学学会-临床医学研究中心
发布:广东省临床医学学会-临床医学研究中心